|
|

樓主 |
發表於 2016-8-22 14:28:56
|
顯示全部樓層
本帖最後由 p470121 於 2016-8-22 14:30 編輯
轉貼2016年4月8日《先探投資週刊》1877期,供同學參考
揭開ASCO的面紗
【文/饒秀真】
在台灣投資生技股,不論是基本面或是操作手法都很「博大精深」,不但考驗投資機構的研究實力,對一般投資人來說更是看得霧煞煞,尤其不可思議的是一家公司的解盲竟能讓台灣最高學術研究機構的院長「嚇」到辭職。對我們來說,也只得追著公司每天不同的說法與不同的事件來分析。
近來最熱與最令人混淆的話題是美國臨床腫瘤學會(American Society of Clinical Oncology, ASCO),尤其是浩鼎宣布可以在ASCO口頭發表OBI-822台灣二/三期臨床試驗(台灣法規失敗)的論文,除了公司在記者會上大力作多演出、試圖激勵投資人外,媒體報導也開始「各自表述」,新聞標題有「浩鼎解盲論文獲ASCO肯定」、「浩鼎重大訊息有啥好振奮的?」、「浩鼎獲ASCO邀請股價直奔漲停」、「浩鼎新藥論文獲ASCO認可」,這些「肯定」與「認可」的字眼都好像在暗示投資人「安」啦!一副到ASCO作口頭報告就是贏家的態勢,不過最近美國三期臨床失敗的台灣北極星藥業(F-PG,6550)雖沒有暫時停止交易,但也確定要去ASCO作口頭報告,生產牛樟芝的國鼎也正在等候ASCO的通知。
如果認為到ASCO對公司是一種「鍍金」,恐怕是一廂情願對ASCO有過度激情的想法!
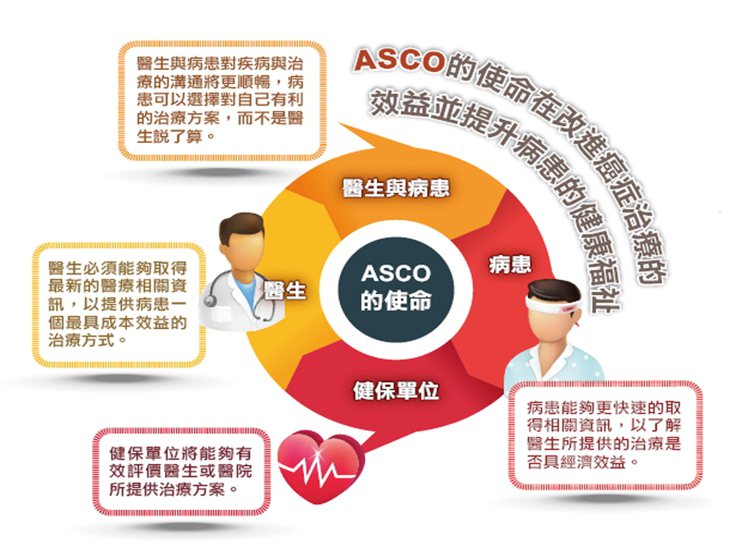
醫療資訊交流平台
ASCO是領先全球的腫瘤癌症研究機構,成員包含了專業的臨床醫師以及癌症研究人員。一九六四年,由Fred Ansfield博士等創立至今,ASCO來自全球超過二.七萬名會員設立了癌症醫療服務的標準,每年來自一百個國家、超過三萬人與會,逾四千名科學家都來發表最新的癌症治療與診斷新方向,同時從過去的歷史來看,到ASCO發表數據的確對公司股價會有影響,也稱作「ASCO Effect」。
其實,ASCO就是一個抗癌的武林大會,四面八方人士都會參與相互觀摩學習。學會召開前會接受各方投稿,評審方面則邀請各國學者專家加入學術委員會擔任委員,遴選可以在學會上交流的論文;論文分為口頭報告、壁報討論和壁報展示。
基本上ASCO就是一個重要的醫療資訊交換平台,聽聽各方批評與意見以求改進,也看看有沒有商業合作的機會,但絕不等於新治療就一定成功,更不是藥證取得的保證。更何況,不要說提出的數據不夠好會影響公司的股價,縱使提出好的臨床數據,但低於市場的預期,或是競爭者的數據更好,都會導致公司的股價大跌。
根據媒體的報導,參加過學會論文發表的學者專家指出,像ASCO這種極具國際聲譽的學會,能上台口頭報告當然很傑出,一般能通過審查的論文,除了有重大研究成果之外,偶爾也會被申請者的學術地位與評審委員的交際關係影響。暗示著OBI-822在有國際名聲與人脈的台灣中研院院長翁啟惠的加持之下,應該閉著眼睛都會通過審查取得報告的資格,這也是翁院長最重要的價值之一,不過專業人士認為應與「關係」無關,單純就是因為過去醣分子在癌症的治療都失敗,所以想了解浩鼎有何不同之處。
台灣的北極星藥業從二○一三~一五年都參加ASCO,也都有口頭報告,該公司無論是藥物開發或是與國際首屈一指專科醫師的臨床實驗合作更豐富,今年更是有三份臨床實驗的論文發表,包括肝癌(Plenary Oral Presentation較大型口頭報告)、肺間皮癌(Poster Discussion Section而不是只有一般壁報發表)與胰臟癌(刊登論文),不過公司只有重訊公告並沒有「刻意」停止交易,也沒大剌剌開記者會或法說會宣揚,顯得低調很多,因為ASCO發表並不代表取得藥證。此外令人印象深刻的是,該公司的美國三期失敗(比台灣三期的價值大多了,因為台灣三期充其量不過是美國的二期)的法說,公司與投資界分享的是臨床失敗的發現,並告知未來三期的新方向與啟動的時程表,而不是還在秘密計畫中,這是比較務實的作法。
值得注意的是,高藥價已經成為全球政府保健支出的沉痛負擔,所以近期ASCO也推出一個評價藥物價格的機制(The ASCO Value Framwork),評分標準是以藥物的治療效果、副作用(毒性)與費用作出來評估新癌症藥物的價值,給醫生與病患作參考,同時未來將提供更方便病患與醫生使用的移動式的App應用以利推廣。
新癌症藥物價值的評估分數在○~一○○分,少數方案因為贏過標準療法等有加分,最高可達到一三○分。在二○一五年六月二十二日出版的《臨床腫瘤學》雜誌(Journal of Clinical Oncology)中,評分嚴格的ASCO將大藥廠羅氏公司的Avastin在肺癌適應症上打了一六分,賽諾菲的前列腺癌藥物Jevtana也只有一六分,得分最高的抗癌藥是一個治療HER2陽性乳癌的賀癌平得最高的四八分。也就是說,未來抗癌藥物市場的競爭將更趨激烈與透明,也就是說想要訂高藥價可不是公司自己說了算,這是研發新藥公司應該要密切追蹤的。
全球抗癌藥研發者湧向ASCO會議,分享他們最新的藥物臨床試驗結果,這些結果對他們公司的下一步發展有著重大影響,甚至會關係到某些公司的生死存亡。所以每年的ASCO除了會定調最新抗癌藥物的發展趨勢外,來自各方的國際法人機構的研究員也會評估市場新的贏家與輸家。
一般來說,ASCO大會數據的發表對公司股價的影響,大廠股價漲幅較難有上天下地的表現,除了二○一五年的施貴寶例外,反而小型股的起伏更大,在這裡與大家分享二○一五年ASCO公司股價的輸家與贏家。
輸家與贏家
浩鼎在記者會特別提到,近年來免疫療法藥物,包括Yervoy、Opdivo及Keytruda等都在ASCO發表第一手資料受矚目。話雖沒錯,以上的新藥幾乎都是拿到數個「突破性性療法」或是「優先審查」資格的重量級新藥,尤其Opdivoe市場潛力呼聲最高,所以市場都在等待即將公布讓人「眼珠子會掉出來」的數據,更期待公司股價可以一飛沖天,尤其二○一五年PD-1/PD-L1的議題火到爆,市場關注施貴寶、默克與羅氏大藥廠,但沒想到施貴寶卻「鍍金不成踩到屎」!成為二○一五年ASCO的大輸家。
主因是施貴寶Opdivo作為二線非小細胞肺癌的三期臨床數據,雖比對照組歐洲紫杉醇的中值生存期延長二.八個月,且對PD-L1陽性患者還多出八個月(一七個月比九個月),很優的臨床數據,但是比投資人的預期差,數據一發表當天股價就大跌六.五%,七○億美元相當兩個浩鼎的市值一夕消失,而Opdivo的主要競爭者Keytrduda公司默克股票則上揚二%(翹翹板效應),施貴寶從五月十三日數據摘要公布到ASCO會議結束期間,股價總計下跌二%。
在此提醒大家注意,Opdivo不是數據不好,只是如果之前投資人期望太高,結果不如預期就會導致股價重挫,而台灣的基亞與浩鼎都是很好的案例,尤其美國資本市場專家一堆,很難用公關宣傳來激勵投資人。當然更要注意的是競爭者的臨床實驗數據,或是同類新產品的提早上市,當初台微體股價的重挫就是印度Sun Pharma的抗乳癌學名藥出乎意料地提早台微體上市。
【本文未完,全文詳情及圖表請見《先探投資週刊》1877期;訂閱先探投資週刊電子版】
評析 ASCO就是一個重要的醫療資訊交換平台,但絕不等於新治療就一定成功,更不是藥證取得的保證。
|
|